В природе есть множество различных веществ, каждое из которых может находиться в одном из трех агрегатных состояний: газе, жидкости или твердом теле. Агрегатное состояние вещества зависит от температуры и давления, которым оно подвергается.
Газ - это состояние вещества, в котором его молекулы находятся на большом расстоянии друг от друга и движутся в хаотичном порядке. Газы обладают свойством легкости и проникают в любую емкость или пространство. Они имеют свободную форму и объем, а также расширяются при нагревании и уменьшаются при охлаждении.
Жидкость - это состояние вещества, в котором его молекулы находятся близко друг к другу и имеют слабые межмолекулярные силы. Жидкости обладают свойствами текучести и плотности. Они имеют форму сосуда, в котором находятся, и занимают его в полном объеме. Жидкости могут изменять свою форму под влиянием внешней силы, но сохраняют свой объем.
Твердое тело - это состояние вещества, в котором его молекулы располагаются на некотором расстоянии друг от друга и имеют сильные межмолекулярные силы. Твердые тела обладают свойствами жесткости и несжимаемости. Они имеют определенную форму и объем, которые не изменяются при изменении условий окружающей среды.
Агрегатные состояния веществ
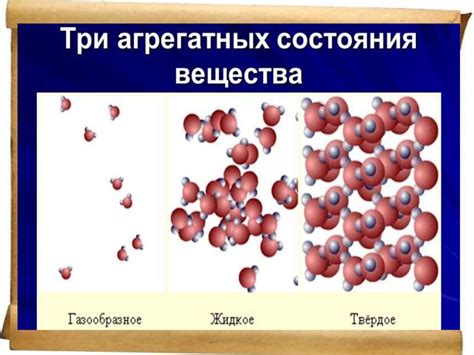
Существует три основных агрегатных состояния вещества:
- Газообразное состояние: вещество находится в виде газа, его молекулы свободно движутся, не имеют постоянной формы и объема. Газы обладают высокой подвижностью и могут заполнять все имеющиеся объемы.
- Жидкое состояние: вещество находится в виде жидкости, его молекулы имеют возможность перемещаться друг относительно друга, но с ограничениями по объему и форме. Жидкости обладают относительной подвижностью и могут заполнять только ограниченные объемы.
- Твердое состояние: вещество находится в виде твердого тела, его молекулы не свободно двигаются, имеют фиксированные положения и не имеют возможности изменять форму и объем. Твердые тела обладают минимальной подвижностью и сохраняют свою форму и объем.
Переходы между агрегатными состояниями вещества могут происходить при изменении температуры и давления. При повышении или понижении температуры или давления вещество может переходить из одного состояния в другое – это называется фазовыми переходами. Например, при нагревании жидкости она может испариться и перейти в газообразное состояние, а при охлаждении газа он может конденсироваться и перейти в жидкое состояние.
Важно отметить, что агрегатные состояния вещества зависят не только от температуры, но и от давления. Например, при достаточно низких температурах и высоком давлении газ может превратиться в жидкость, а при очень низких температурах и высоком давлении жидкость может превратиться в твердое тело.
В итоге, знание об агрегатных состояниях вещества является важной основой для понимания его свойств и поведения в различных условиях.
Газовое состояние
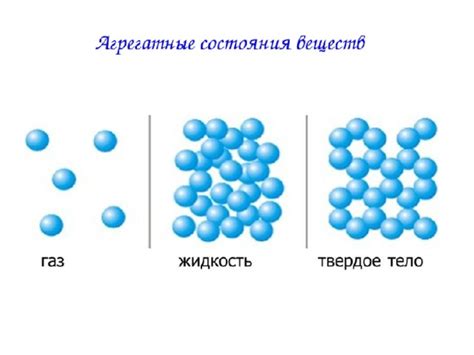
Газы состоят из молекул, которые находятся в постоянном движении. Молекулы газа находятся на значительном расстоянии друг от друга и взаимодействуют слабо. Именно эти свойства обеспечивают газам способность расширяться и сжиматься в зависимости от изменения условий, в которых они находятся.
Одной из основных характеристик газов является их давление. Давление газа возникает в результате столкновений молекул газа с стенками сосуда, в котором он находится. Давление газа зависит от его температуры и объема.
Газы обладают множеством свойств и находят применение в различных областях человеческой деятельности. Среди наиболее известных газов можно назвать кислород, азот, углекислый газ и водород. Газы используются в промышленности, медицине, быту и других сферах.
| Примеры газов | Свойства | Применение |
|---|---|---|
| Кислород | Бесцветный, без запаха, поддерживает горение | Используется в медицине, в процессе сварки и горения |
| Азот | Бесцветный, без запаха, негорючий | Используется в промышленности, в пищевой и химической отраслях |
| Углекислый газ | Бесцветный, горючий, не поддерживает горение | Используется в газоанализе, в процессе огнетушения |
| Водород | Бесцветный, взрывоопасный, легче воздуха | Используется в химической промышленности, в космических исследованиях |
Жидкое состояние

Жидкое состояние обычно сохраняется при комнатной температуре и атмосферном давлении для большинства веществ, однако некоторые вещества могут находиться в жидком состоянии только при определенных условиях температуры и давления.
Основными свойствами жидкости являются:
поверхностное натяжение - способность жидкости образовывать поверхность, например, пузырьки или капли;
вязкость - свойство сопротивляться течению и деформации жидкости;
плотность - отношение массы к объему вещества;
теплоемкость - количество энергии, необходимое для нагревания жидкости на определенную температуру.
В жидком состоянии вещества могут происходить различные химические и физические процессы, такие как растворение, плавление и кристаллизация.
Твердое состояние
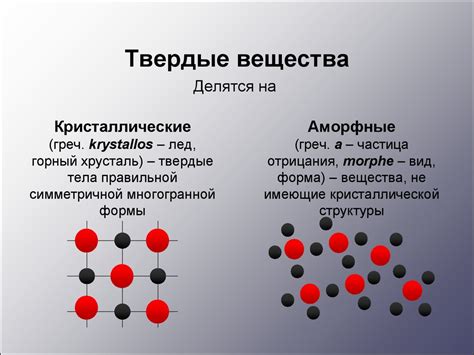
Основным свойством твердых веществ является их жесткость. Она обеспечивает им форму и позволяет сопротивляться деформации. Твердые вещества обладают также высокой плотностью и инерцией. В зависимости от структуры и свойств твердого вещества, оно может быть хрупким или пластичным, прозрачным или непрозрачным.
Примеры твердых веществ включают металлы, камни, дерево, стекло, лед и многие другие материалы. Твердое состояние является наиболее распространенным агрегатным состоянием веществ и встречается в ежедневной жизни повсюду.
Твердые вещества обладают рядом уникальных свойств и находят применение в различных областях. Металлы используются в промышленности и строительстве, дерево - в производстве мебели и строительных материалов, стекло - в производстве окон и посуды, а камни - в ювелирном искусстве.



